El dolor crónico no oncológico afecta a aproximadamente uno de cada cinco adultos a nivel global y constituye una de las primeras causas de discapacidad. Los lineamientos clínicos contemporáneos posicionan al ejercicio físico como intervención de primera línea, con respaldo proveniente de revisiones Cochrane, metaanálisis en red y guías internacionales como las recomendaciones OMS 2020 sobre actividad física.
Esta revisión sintetiza la evidencia acumulada entre 2005 y 2025 en torno a cuatro ejes: los mecanismos neurobiológicos de la hipoalgesia inducida por ejercicio (con énfasis en las vías serotoninérgica y noradrenérgica descendentes, los sistemas opioide y endocannabinoide endógenos, y el factor neurotrófico derivado del cerebro o BDNF); el efecto antiinflamatorio sistémico mediado por la interleuquina-6 como miocina; la evidencia comparada de modalidades específicas (aeróbico, fortalecimiento, mente-cuerpo, marcha); y la prescripción práctica basada en las recomendaciones OMS de 150-300 minutos semanales de actividad de intensidad moderada y dos sesiones semanales de fortalecimiento. La conclusión central es que el ejercicio actúa como modificador real de la fisiopatología del dolor a través de mecanismos validados, con efectividad comparable a fármacos en varias condiciones, perfil de seguridad favorable, y beneficios extramusculares relevantes (sueño, ánimo, función). La adherencia es el factor crítico que determina la magnitud del efecto clínico.
1. Introducción
El dolor crónico no oncológico, definido como dolor persistente más allá del tiempo esperado de cicatrización tisular —generalmente más de doce semanas— afecta aproximadamente al 20% de la población adulta mundial y representa una de las primeras causas de años vividos con discapacidad. La carga global es particularmente elevada en patologías como el dolor lumbar crónico, la artrosis de rodilla y cadera, la fibromialgia y los dolores cervicales persistentes. La evolución conceptual de las últimas dos décadas ha desplazado la mirada desde un modelo puramente nociceptivo hacia un modelo biopsicosocial que reconoce la sensibilización central, la disfunción de las vías inhibitorias descendentes, la inflamación sistémica de bajo grado y los factores afectivos y cognitivos como dimensiones interrelacionadas del dolor crónico.
En este contexto, la prescripción de reposo prolongado —recomendación tradicional durante décadas— ha sido reemplazada por una indicación inversa: el movimiento activo y estructurado se considera hoy intervención de primera línea, con grado de recomendación fuerte y evidencia de certeza moderada a alta en las principales guías clínicas internacionales, incluida la guía OMS 2023 para el manejo no quirúrgico del dolor lumbar crónico primario. La inactividad física no solo no protege al paciente con dolor crónico: la sostiene, la amplifica y le añade comorbilidades cardiovasculares, metabólicas y emocionales.
Esta revisión narrativa busca integrar la evidencia actual sobre el ejercicio en dolor crónico no oncológico desde tres ángulos complementarios: el mecanístico (cómo el movimiento modula el dolor a nivel neurobiológico e inmunológico), el clínico (qué modalidades, dosis y formatos han demostrado eficacia en ensayos controlados aleatorizados y metaanálisis) y el aplicativo (cómo trasladar esta evidencia a la prescripción concreta del paciente, incluyendo el ejercicio domiciliario).
2. La paradoja de la inactividad: cuando el reposo perpetúa el dolor
La relación entre sedentarismo y dolor crónico es bidireccional. Por una parte, la inactividad física prolongada produce desacondicionamiento muscular, pérdida de masa magra, reducción de densidad mineral ósea, deterioro de las estructuras musculotendinosas por privación de carga mecánica, y alteraciones degenerativas del sistema nervioso1. Por otra, el dolor genera conductas de evitación (modelo fear-avoidance descrito por Lethem y validado posteriormente por Vlaeyen y Linton) que reducen progresivamente la actividad y consolidan un círculo vicioso de pérdida funcional2. A nivel poblacional, se estima que aproximadamente uno de cada cuatro adultos no alcanza los niveles mínimos de actividad física recomendados por la Organización Mundial de la Salud, una cifra que se duplica entre los adolescentes1,3.
Este fenómeno tiene implicancias mecanísticas concretas: la pérdida de masa muscular reduce la capacidad endocrina del músculo esquelético —hoy reconocido como órgano endocrino activo productor de miocinas con efectos sistémicos antiinflamatorios y neurotróficos—, comprometiendo así uno de los principales mecanismos endógenos de modulación del dolor4,5. La inactividad también compromete la función de los sistemas serotoninérgico y noradrenérgico descendentes, que constituyen la vía principal de inhibición fisiológica del dolor a nivel medular y supramedular6,7.
◆ Evidencia central
La revisión paraguas de Geneen y colaboradores (Cochrane Database 2017), que sintetizó 21 revisiones sistemáticas Cochrane previas con un total de 381 ensayos clínicos y más de 37.000 participantes, concluyó que el ejercicio y la actividad física producen mejoras pequeñas a moderadas en intensidad de dolor y función física en adultos con dolor crónico, con un perfil de seguridad favorable y efectos adversos infrecuentes y leves.
3. Mecanismos neurobiológicos de la hipoalgesia inducida por ejercicio
La hipoalgesia inducida por ejercicio (exercise-induced hypoalgesia, EIH) es un fenómeno descrito desde la década de 1980 que se refiere al aumento en los umbrales de dolor y la reducción de la sensibilidad nociceptiva tras una sesión aguda de actividad física, con efectos que pueden persistir minutos a horas después del ejercicio. La EIH se ha documentado consistentemente en sujetos sanos y, con respuesta más heterogénea, en poblaciones con dolor crónico. Sus mecanismos son múltiples y complementarios.
3.1 Sistemas opioide y endocannabinoide endógenos
El sistema opioide endógeno fue históricamente la primera explicación propuesta para la EIH. El ejercicio, particularmente aeróbico de intensidad moderada-alta y de duración suficiente, induce liberación de β-endorfina y met-encefalina en la sustancia gris periacueductal y la médula rostral ventromedial —los dos núcleos centrales del sistema descendente de modulación del dolor—8. Sin embargo, los antagonistas opioides como naloxona solo bloquean parcialmente el efecto analgésico del ejercicio, lo que motivó la búsqueda de mecanismos adicionales.
El sistema endocannabinoide ha emergido como segundo eje fundamental. Estudios en modelos animales y humanos han demostrado que el ejercicio aumenta los niveles plasmáticos de anandamida (N-araquidoniletanolamina) y 2-araquidonoilglicerol, ligandos endógenos de los receptores CB1 y CB29. El bloqueo farmacológico de estos receptores con antagonistas como AM251 y AM630 elimina la antinocicepción inducida por ejercicio, confirmando un rol causal del sistema endocannabinoide en la EIH9.
3.2 Sistemas serotoninérgico y noradrenérgico descendentes
Las vías descendentes serotoninérgicas (5-HT) y noradrenérgicas (NE) constituyen el sustrato neuroquímico principal de la modulación inhibitoria del dolor a nivel medular. El núcleo del rafe magno (5-HT) y el locus coeruleus (NE) proyectan hacia las astas dorsales de la médula espinal, donde modulan la transmisión de las señales nociceptivas. Esta vía es, no por casualidad, el blanco terapéutico de los inhibidores duales de recaptura de serotonina y noradrenalina (duloxetina, venlafaxina) utilizados en dolor crónico, fibromialgia y dolor neuropático.
Es necesario distinguir con rigor entre la evidencia humana y la animal sobre la activación de estos sistemas durante el ejercicio. En humanos la evidencia es indirecta y proviene de tres líneas: el aumento del cociente plasmático free-tryptophan/aminoácidos de cadena ramificada durante el ejercicio prolongado, que incrementa la captación cerebral de triptófano vía el transportador LAT-1 de la barrera hematoencefálica28,29; la elevación de noradrenalina plasmática proporcional a intensidad y duración (1,5 a más de 20 veces el valor basal en ejercicio intenso, principalmente de origen simpático periférico y medular adrenal, no del locus coeruleus)30,31; y la respuesta clínica al ejercicio en cuadros de sensibilización central, evaluada mediante la modulación condicionada del dolor (conditioned pain modulation o CPM) como proxy de la función inhibitoria descendente11. La medición directa de 5-HT cerebral en humanos es metodológicamente inviable (la microdiálisis cerebral está restringida a contextos neuroquirúrgicos), por lo que la evidencia mecanística directa proviene de modelos animales.
En modelos murinos, Bobinski y colaboradores demostraron en Pain (2015) que el ejercicio en cinta de baja intensidad en ratones con neuropatía del nervio ciático aumenta la concentración de 5-HT y la expresión de sus receptores 5-HT1B, 5-HT2A y 5-HT2C, y disminuye la expresión del transportador SERT en el tronco encefálico, con reducción concomitante de la hiperalgesia mecánica6. Lopez-Alvarez y colegas extendieron este hallazgo demostrando que el ejercicio progresivo en cinta tras lesión nerviosa periférica modula también la vía noradrenérgica descendente10. Estudios complementarios de microdiálisis han documentado aumentos del 47% en 5-HT extracelular hipocampal tras una hora de ejercicio en cinta, y up-regulación de receptores 5-HT1A en el núcleo dorsal del rafe tras entrenamiento crónico32,33.
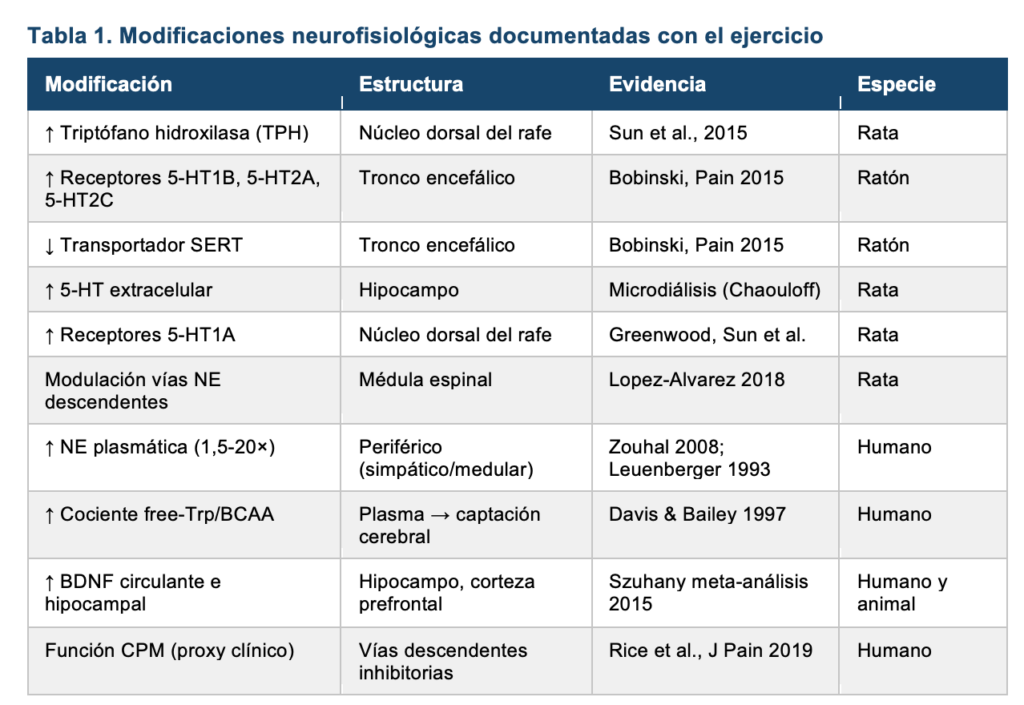
▸ Implicancia clínica
El ejercicio aeróbico regular activa los sistemas serotoninérgico y noradrenérgico centrales mediante mecanismos endógenos que reproducen, en parte, el blanco terapéutico de los antidepresivos duales (IRSN). Esto fundamenta su rol como intervención de primera línea en cuadros con sensibilización central como fibromialgia, dolor lumbar crónico inespecífico, cefalea tensional crónica y síndromes de dolor regional complejo, especialmente cuando coexisten síntomas afectivos. La heterogeneidad de respuesta entre pacientes con función CPM disminuida obliga a un escalamiento prudente de intensidad.
3.3 BDNF y neuroplasticidad
El factor neurotrófico derivado del cerebro (brain-derived neurotrophic factor, BDNF) es una neurotrofina central en la plasticidad sináptica, la neurogénesis hipocampal y la modulación nociceptiva. El ejercicio aeróbico de intensidad moderada a alta induce incrementos significativos de BDNF circulante y central, particularmente en el hipocampo y la corteza prefrontal12, con un efecto bidireccional: el BDNF potencia la señalización serotoninérgica y, recíprocamente, la serotonina aumenta la expresión de BDNF, configurando un eje funcional clave para la analgesia y la regulación del ánimo13.
Lee y colaboradores demostraron en un ensayo controlado en mujeres premenopáusicas con dolor lumbar crónico que doce semanas de práctica de yoga (tres sesiones semanales) reducen significativamente la intensidad del dolor (escala analógica visual) e incrementan los niveles séricos de BDNF, mientras que el grupo control mostró tendencia inversa13. Este hallazgo es consistente con un creciente cuerpo de evidencia que posiciona al BDNF como mediador molecular candidato del efecto analgésico y antidepresivo del ejercicio.
3.4 Sistema de recompensa mesolímbico
Estudios recientes en modelos murinos de dolor neuropático han demostrado que el ejercicio voluntario activa neuronas glutamatérgicas en la amígdala basal medial proyectadas al núcleo accumbens (vía mesocorticolímbica de recompensa) y suprime la activación GABAérgica inducida por dolor en el núcleo central de la amígdala14. Esta modulación afectivo-emocional del dolor es particularmente relevante en pacientes con kinesiofobia y catastrofización, en quienes el componente emocional amplifica la experiencia dolorosa.
4. El efecto antiinflamatorio sistémico: la interleuquina-6 como miocina
Uno de los hitos conceptuales más relevantes en la última década ha sido la caracterización del músculo esquelético como órgano endocrino activo productor de miocinas —citocinas y péptidos liberados por la fibra muscular en contracción que ejercen efectos paracrinos y endocrinos sistémicos—. Bente Klarlund Pedersen y su grupo en Copenhague identificaron en el año 2000 a la interleuquina-6 (IL-6) como la primera miocina4, y desde entonces se han descrito más de cien miocinas adicionales, incluyendo irisina, IL-15, BDNF, catepsina B y FGF21.
La IL-6 producida por el músculo durante el ejercicio (que puede aumentar hasta cien veces sus niveles basales en una sesión prolongada) tiene un comportamiento opuesto al de la IL-6 producida por el tejido adiposo o por monocitos en un contexto séptico. La IL-6 muscular estimula la liberación de IL-1ra (antagonista del receptor de IL-1) e IL-10 —dos citocinas antiinflamatorias clásicas— e inhibe la producción de TNF-α, principal motor de la inflamación sistémica de bajo grado4,5. Esta dualidad fue elegantemente demostrada en un experimento de laboratorio en humanos: la administración de endotoxina bacteriana en sujetos sedentarios produjo un aumento de dos a tres veces en los niveles de TNF-α, mientras que en sujetos que realizaron tres horas de ergómetro previas a la administración de endotoxina la respuesta de TNF-α quedó completamente abolida4.
Una revisión sistemática y metaanálisis de 23 ensayos controlados aleatorizados publicada en 2025 evaluó el efecto del ejercicio sobre marcadores inflamatorios en pacientes con dolor musculoesquelético. El metaanálisis demostró reducciones estadísticamente significativas en proteína C reactiva (diferencia media -0,40, IC 95%: -0,44 a -0,36), IL-6 (DM -1,59, IC 95%: -2,61 a -0,56) y TNF-α (DM -4,24, IC 95%: -5,13 a -3,36) cuando se comparó ejercicio isocinético contra ejercicio general15. Estos hallazgos sostienen la hipótesis de que el ejercicio actúa como antiinflamatorio sistémico real, no solo a través de mecanismos mecánicos locales sino mediante la modulación del eje músculo-tejido adiposo-sistema inmune.
◆ Mecanismo clave
La IL-6 producida por el músculo en contracción es antiinflamatoria; la IL-6 producida por el tejido adiposo visceral en obesidad o por monocitos en sepsis es proinflamatoria. La misma molécula tiene efectos opuestos según su origen y contexto. Esto explica por qué el ejercicio regular reduce los marcadores inflamatorios crónicos pese a generar elevaciones agudas de IL-6 durante cada sesión.
5. Marco normativo: recomendaciones OMS 2020 sobre actividad física
Las WHO Guidelines on Physical Activity and Sedentary Behaviour, publicadas en noviembre de 2020 y vigentes a la fecha, constituyen el marco internacional de referencia. Las recomendaciones para adultos (incluidos los que viven con condiciones crónicas o discapacidad) son las siguientes1,3:
• Realizar al menos 150 a 300 minutos semanales de actividad física aeróbica de intensidad moderada, o 75 a 150 minutos semanales de intensidad vigorosa, o una combinación equivalente de ambas. Recomendación fuerte, certeza moderada de evidencia.
• Realizar actividades de fortalecimiento muscular de intensidad moderada o mayor, que involucren todos los grandes grupos musculares, en dos o más días a la semana. Recomendación fuerte, certeza moderada.
• En adultos mayores, incorporar adicionalmente actividades multicomponente que incluyan equilibrio funcional y entrenamiento de fuerza al menos tres días por semana, para reducir riesgo de caídas.
• Limitar el tiempo sedentario y reemplazarlo por actividad física de cualquier intensidad. Cualquier cantidad de actividad es preferible a ninguna.
Una actualización conceptual relevante de la guía 2020 fue la eliminación del requisito histórico de que la actividad debía acumularse en bouts de al menos diez minutos: la evidencia actual demuestra que sesiones cortas son igualmente efectivas, lo que tiene implicancias prácticas importantes para pacientes con dolor crónico que pueden no tolerar sesiones prolongadas y se benefician de un enfoque snacking o fragmentado a lo largo del día3. La guía OMS 2023 específica para dolor lumbar crónico primario reafirma estas recomendaciones generales y agrega indicaciones específicas para esta población.
6. Ejercicio aeróbico: evidencia y prescripción
El ejercicio aeróbico —definido como actividad continua que eleva la frecuencia cardíaca y respiratoria por períodos prolongados— ha sido extensamente estudiado en dolor crónico. Su efecto analgésico ha sido vinculado a la activación de los sistemas opioide, endocannabinoide, serotoninérgico y noradrenérgico previamente descritos, así como a la elevación de BDNF y a la regulación de la función autonómica6,12,16.
Pocovi y colaboradores publicaron en The Lancet (junio 2024) los resultados del estudio WalkBack, un ensayo controlado aleatorizado pragmático con 701 adultos australianos recientemente recuperados de un episodio de dolor lumbar inespecífico, quienes fueron asignados a un programa individualizado y progresivo de caminata combinado con educación versus control sin tratamiento17. El programa redujo el riesgo de recurrencia limitante de actividad en un 28% y la búsqueda de atención sanitaria por dolor lumbar en un 43%, con una mediana de tiempo libre de dolor de 208 días en el grupo intervención versus 112 días en el grupo control. Adicionalmente, la intervención fue costo-efectiva desde la perspectiva social. Este es el primer ensayo aleatorizado de adecuado poder estadístico que demuestra la efectividad de la caminata como estrategia de prevención secundaria del dolor lumbar.
La intensidad óptima para EIH ha sido objeto de debate. La revisión paraguas de Polaski y colaboradores publicada en PLoS ONE (2019) sugiere que el ejercicio aeróbico de intensidad moderada (60-70% de la frecuencia cardíaca máxima o de la reserva de frecuencia cardíaca) durante al menos 30 minutos produce efectos analgésicos consistentes en pacientes con dolor crónico18. Intensidades muy bajas tienden a ser insuficientes para activar los mecanismos antinociceptivos centrales, mientras que intensidades muy altas pueden producir hiperalgesia paradojal en pacientes con sensibilización central marcada o con función inhibitoria descendente comprometida.
▸ Prescripción práctica · ejercicio aeróbico
Modalidad: caminata, bicicleta estática o paseante, natación, elíptica, o ejercicio acuático según tolerancia articular.
Frecuencia: 3 a 5 sesiones semanales, idealmente distribuidas (no agrupadas en fin de semana).
Duración: progresar gradualmente desde 10 minutos por sesión hasta 30-50 minutos según tolerancia. Pacientes muy desacondicionados pueden iniciar con 3-5 minutos varias veces al día.
Intensidad objetivo: 60-70% de la frecuencia cardíaca de reserva, o nivel donde la persona puede mantener una conversación pero no cantar (talk test). Duración total semanal objetivo: alcanzar progresivamente 150 minutos de moderada (recomendación OMS) en un plazo de 8-12 semanas.
7. Fortalecimiento muscular: evidencia y prescripción
El entrenamiento de resistencia (resistance training) es una intervención robustamente respaldada en múltiples condiciones de dolor crónico. La debilidad muscular es a la vez consecuencia y causa de progresión del dolor: en artrosis de rodilla, por ejemplo, la disminución de la fuerza del cuádriceps reduce la capacidad de absorción de carga de la articulación e incrementa la rigidez articular, generando un círculo vicioso bien documentado19.
En artrosis de rodilla y cadera, una revisión sistemática y metaanálisis de 17 ensayos controlados aleatorizados (1.705 pacientes) demostró que el entrenamiento de resistencia reduce significativamente el dolor, mejora la función física y disminuye la rigidez articular20. Una revisión sistemática actualizada de 2024 confirma que el entrenamiento de fuerza, de cualquier modalidad (isométrico, isotónico o isocinético), produce mejoras consistentes en dolor, fuerza y función, con el isocinético mostrando la mejor relación efecto-comparador en metaanálisis en red19.
En fibromialgia, el entrenamiento de resistencia ha demostrado eficacia en reducción de dolor, fatiga, depresión y mejoría de la función física. El metaanálisis de Andrade y colegas (Clinical Rheumatology 2023), que incluyó 13 ensayos aleatorizados y 530 pacientes, encontró reducciones favorables en el cuestionario de impacto de fibromialgia (FIQ), intensidad del dolor, número de puntos dolorosos y síntomas depresivos comparado con grupo control sin intervención21. Una revisión sistemática complementaria publicada en 2025 sugiere que el entrenamiento progresivo iniciado a baja intensidad (40% de 1RM) es la prescripción inicial más adecuada en fibromialgia, escalando progresivamente hacia intensidad moderada según tolerancia22.
El metaanálisis en red de Hayden y colaboradores publicado en Journal of Physiotherapy (2021), que incluyó 217 ensayos y casi 21.000 participantes, mostró que en dolor lumbar crónico todas las modalidades de ejercicio fueron superiores al tratamiento mínimo, pero Pilates, terapia McKenzie y restauración funcional tuvieron los efectos más consistentes en reducción de intensidad de dolor y limitaciones funcionales23. Este hallazgo es relevante: en ausencia de contraindicaciones específicas, la modalidad de ejercicio que el paciente prefiere y mantiene suele ser superior a la modalidad teóricamente más eficaz pero abandonada precozmente.
▸ Prescripción práctica · fortalecimiento
Frecuencia: 2 sesiones semanales no consecutivas (recomendación OMS).
Volumen inicial: 1-2 series de 8-12 repeticiones por ejercicio, abarcando los grandes grupos musculares (cuádriceps, glúteos, abductores, extensores espinales, dorsal ancho, deltoides).
Intensidad inicial: 40-50% de 1RM en pacientes desacondicionados o con sensibilización central; progresar hacia 60-80% según tolerancia, en plazo de 4-12 semanas.
Modalidad: bandas elásticas, peso corporal, mancuernas livianas, máquinas guiadas. La utilización de carga restringida de flujo sanguíneo (BFR) es una alternativa emergente para pacientes con limitación de carga articular alta. Progresión: regla de la sobrecarga progresiva. Cuando la persona completa la serie alta del rango de repeticiones con técnica adecuada, aumentar carga 5-10%.
8. Ejercicio mente-cuerpo: yoga, tai chi y Pilates
Las modalidades mente-cuerpo integran movimiento, control respiratorio y atención focalizada. Su evidencia en dolor crónico ha crecido sustancialmente en la última década. La revisión sistemática y metaanálisis de Kong y colaboradores publicada en Scientific Reports (2016), que incluyó 18 ensayos controlados aleatorizados, demostró que el tai chi produce alivio inmediato del dolor en artrosis (diferencia media estandarizada -0,54, IC 95%: -0,77 a -0,30), dolor lumbar crónico (DME -0,81, IC 95%: -1,11 a -0,52) y osteoporosis (DME -0,83, IC 95%: -1,37 a -0,28), con duración mínima efectiva de cinco a seis semanas24.
Para Pilates, la evidencia es particularmente robusta en dolor lumbar. El metaanálisis en red de Pozuelo-Carrascosa y colaboradores publicado en JOSPT (2022) posicionó a Pilates como la modalidad con mayor reducción de intensidad de dolor en dolor lumbar crónico al compararla cabeza a cabeza con otras modalidades25. La actualización del metaanálisis Cochrane de Hayden 2021 mostró que Pilates redujo el dolor en mayor magnitud que estiramientos, ejercicio aeróbico, mixto, fortalecimiento general, yoga, restauración funcional y core strengthening (DM entre -12 y -4 puntos en escala 0-100, certeza baja a moderada)23.
El yoga, además de los efectos analgésicos descritos, induce cambios neurobiológicos medibles: el ensayo de Lee y colegas (2014) mostró aumentos significativos de BDNF sérico y mantención de niveles de serotonina tras doce semanas de práctica en mujeres con dolor lumbar crónico13, lo que sugiere que sus efectos exceden los componentes mecánicos de movilidad y van hacia la modulación neuroquímica.
▸ Prescripción práctica · mente-cuerpo
Indicación preferente: pacientes con sensibilización central, fibromialgia, dolor lumbar crónico inespecífico, kinesiofobia, comorbilidad afectiva, adultos mayores con riesgo de caídas (tai chi).
Frecuencia: 2-3 sesiones semanales de 45-60 minutos.
Duración mínima para efecto clínicamente significativo: 6-12 semanas. Adaptación: priorizar instructores con formación en poblaciones clínicas; evitar posturas de carga axial o flexiones forzadas en pacientes con patología degenerativa avanzada o inestabilidad.
9. Caminar: la intervención más accesible y subutilizada
La caminata merece una sección propia por dos razones: es la modalidad más accesible (sin costo, sin equipamiento, replicable en cualquier contexto urbano o rural) y, hasta el ensayo WalkBack, había sido sorprendentemente poco estudiada como intervención formal. El estudio publicado en The Lancet en 2024 cambió el panorama: en pacientes recuperados de un episodio de dolor lumbar, una intervención de caminata progresiva e individualizada combinada con educación durante seis meses redujo recurrencias en 28%, búsqueda de atención sanitaria en 43%, y duplicó el tiempo libre de dolor (mediana 208 versus 112 días)17.
Los mecanismos propuestos para la efectividad de la caminata son la combinación de movimientos oscilatorios suaves que cargan y fortalecen las estructuras espinales y la musculatura paravertebral, la liberación de endorfinas, la reducción del estrés y la mejora del sueño y del peso corporal —todos factores que modulan el dolor crónico17,26. A nivel cardiovascular y metabólico, la caminata regular reduce mortalidad por todas las causas, riesgo de enfermedad cardiovascular, diabetes tipo 2 y depresión, lo que potencia su valor en una población —la del dolor crónico— frecuentemente caracterizada por multimorbilidad.
10. Adherencia: el factor crítico
Toda la evidencia previa converge en una observación operacional: la magnitud del efecto del ejercicio en dolor crónico depende críticamente de la adherencia. Un análisis secundario del metaanálisis Cochrane de Hayden (publicado en Journal of Physiotherapy 2025), que incluyó 46 ensayos y 56 grupos de ejercicio, demostró una relación dosis-respuesta clara: alta adherencia (80-100%) se asoció a reducción de dolor de 14,3 puntos en escala 0-100 (IC 95%: 10,0 a 18,6) y reducción de limitaciones funcionales de 8,1 puntos; adherencia moderada (60-79%) no se asoció a mejorías estadísticamente significativas27.
Esto tiene una implicancia clínica directa: la elección de modalidad debe ponderar fuertemente la preferencia y sostenibilidad para el paciente, incluso cuando otra modalidad teóricamente sea superior por evidencia. Un programa de Pilates con 30% de adherencia produce menos beneficio que un programa de caminata con 90% de adherencia. La integración de educación en neurociencia del dolor, expectativas realistas, autoeficacia y soporte social es tan relevante como la prescripción de ejercicio en sí.
⚠ Pacientes con sensibilización central: precaución
En pacientes con función inhibitoria descendente comprometida (CPM disminuida, hiperalgesia generalizada), el ejercicio de alta intensidad puede producir hiperalgesia paradojal y empeoramiento sintomático. La estrategia recomendada en estos casos es iniciar con baja intensidad, priorizar modalidades con componente afectivo-cognitivo (yoga, tai chi), monitorizar respuesta los primeros 7-10 días, y progresar muy gradualmente. La regla del ’24 horas’ (el ejercicio no debe producir dolor que persista más de 24 horas) sigue siendo una guía clínica útil.
11. Aplicación clínica integrada
La traducción de esta evidencia a la práctica clínica requiere un enfoque individualizado pero estructurado. Una propuesta operacional consiste en tres pilares simultáneos: aeróbico, fortalecimiento y movilidad/mente-cuerpo.
El componente aeróbico cubre los 150-300 minutos OMS y aporta el efecto antiinflamatorio sistémico vía IL-6 muscular, la activación de vías opioide y endocannabinoide, y la elevación de BDNF. Caminata, bicicleta estática y natación son las opciones de mayor accesibilidad y menor riesgo articular.
El componente fortalecimiento cubre las dos sesiones semanales de fuerza recomendadas y aborda específicamente la pérdida de masa magra (sarcopenia funcional o asociada a edad), un mediador importante del dolor en artrosis y dolor lumbar. Bandas elásticas, peso corporal y mancuernas livianas son suficientes para iniciar.
El componente movilidad y mente-cuerpo aporta beneficio en kinesiofobia, regulación del estrés, sueño y modulación afectiva del dolor. Yoga, tai chi y Pilates son las modalidades con mejor evidencia.
La combinación de los tres pilares en formato multicomponente ha demostrado ser superior a cualquier modalidad aislada, particularmente en fibromialgia, donde el metaanálisis en red de la EULAR posiciona la combinación aeróbico + fortalecimiento como la prescripción de elección.
12. Conclusiones
La evidencia acumulada en las últimas dos décadas establece al ejercicio físico como intervención central, no auxiliar, en el manejo del dolor crónico no oncológico. Su efectividad ha sido demostrada en revisiones Cochrane, metaanálisis en red, ensayos de gran escala publicados en revistas de máximo impacto, y guías clínicas internacionales con recomendación de fuerza alta.
Los mecanismos involucrados son múltiples y complementarios: activación de los sistemas opioide y endocannabinoide endógenos; modulación de las vías serotoninérgica y noradrenérgica descendentes —el mismo sustrato que utilizan los antidepresivos duales—; elevación de BDNF y promoción de neuroplasticidad; activación del sistema mesolímbico de recompensa; y reducción de la inflamación sistémica de bajo grado mediada por la IL-6 producida por el músculo en contracción y otras miocinas.
La prescripción ideal combina los tres pilares —aeróbico, fortalecimiento y mente-cuerpo o movilidad— alineados con las recomendaciones OMS 2020 de 150-300 minutos semanales de actividad moderada y dos sesiones de fortalecimiento. La intensidad y progresión deben ser individualizadas según la condición, el grado de sensibilización central y las preferencias del paciente. La caminata progresiva, validada como prevención secundaria del dolor lumbar en el estudio WalkBack, constituye una opción de altísimo valor por su accesibilidad universal.
La adherencia es el factor que determina la magnitud del efecto clínico. La elección de modalidad debe priorizar la sostenibilidad sobre la superioridad teórica. La integración de educación en neurociencia del dolor, manejo de expectativas, abordaje de kinesiofobia y soporte social potencia el efecto del ejercicio per se.
El ejercicio no es alternativa al manejo intervencionista, farmacológico o psicológico del dolor crónico: es la base sobre la que estos otros pilares se sostienen. Como ha sido frecuentemente formulado en la literatura, el ejercicio en dolor crónico es la «mejor medicina» disponible —segura, accesible, costo-efectiva y con beneficios extramusculares relevantes—, y su prescripción rigurosa es responsabilidad del médico clínico.
Referencias
Todas las referencias incluidas han sido verificadas en PubMed, las páginas oficiales de Cochrane Library y The Lancet, o las páginas oficiales de las revistas indexadas correspondientes. Los DOI y PMID se incluyen para identificación inequívoca.
1. World Health Organization. WHO Guidelines on Physical Activity and Sedentary Behaviour. Geneva: World Health Organization; 2020. ISBN 978-92-4-001512-8. Disponible en: https://www.who.int/publications/i/item/9789240015128
2. Vlaeyen JWS, Linton SJ. Fear-avoidance and its consequences in chronic musculoskeletal pain: a state of the art. Pain. 2000;85(3):317-332. doi:10.1016/S0304-3959(99)00242-0. PMID: 10781906.
3. Bull FC, Al-Ansari SS, Biddle S, et al. World Health Organization 2020 guidelines on physical activity and sedentary behaviour. Br J Sports Med. 2020;54(24):1451-1462. doi:10.1136/bjsports-2020-102955. PMID: 33239350.
4. Petersen AMW, Pedersen BK. The anti-inflammatory effect of exercise. J Appl Physiol. 2005;98(4):1154-1162. doi:10.1152/japplphysiol.00164.2004. PMID: 15772055.
5. Pedersen BK. The anti-inflammatory effect of exercise: its role in diabetes and cardiovascular disease control. Essays Biochem. 2006;42:105-117. doi:10.1042/bse0420105. PMID: 17144883.
6. Bobinski F, Ferreira TAA, Córdova MM, et al. Role of brainstem serotonin in analgesia produced by low-intensity exercise on neuropathic pain after sciatic nerve injury in mice. Pain. 2015;156(12):2595-2606. doi:10.1097/j.pain.0000000000000372. PMID: 26447701.
7. Sluka KA, Frey-Law L, Hoeger Bement M. Exercise-induced pain and analgesia? Underlying mechanisms and clinical translation. Pain. 2018;159 Suppl 1:S91-S97. doi:10.1097/j.pain.0000000000001235. PMID: 30113953.
8. Stagg NJ, Mata HP, Ibrahim MM, et al. Regular exercise reverses sensory hypersensitivity in a rat neuropathic pain model: role of endogenous opioids. Anesthesiology. 2011;114(4):940-948. doi:10.1097/ALN.0b013e318210f880. PMID: 21386701.
9. Galdino G, Romero TRL, Silva JFP, et al. The endocannabinoid system mediates aerobic exercise-induced antinociception in rats. Neuropharmacology. 2014;77:313-324. doi:10.1016/j.neuropharm.2013.09.022. PMID: 24148812.
10. Lopez-Alvarez VM, Puigdomenech M, Navarro X, Cobianchi S. Monoaminergic descending pathways contribute to modulation of neuropathic pain by increasing intensity treadmill exercise after peripheral nerve injury. Exp Neurol. 2018;299(Pt A):42-55. doi:10.1016/j.expneurol.2017.10.007. PMID: 29031970.
11. Rice D, Nijs J, Kosek E, et al. Exercise-Induced Hypoalgesia in Pain-Free and Chronic Pain Populations: State of the Art and Future Directions. J Pain. 2019;20(11):1249-1266. doi:10.1016/j.jpain.2019.03.005. PMID: 30904519.
12. Szuhany KL, Bugatti M, Otto MW. A meta-analytic review of the effects of exercise on brain-derived neurotrophic factor. J Psychiatr Res. 2015;60:56-64. doi:10.1016/j.jpsychires.2014.10.003. PMID: 25455510.
13. Lee M, Moon W, Kim J. Effect of yoga on pain, brain-derived neurotrophic factor, and serotonin in premenopausal women with chronic low back pain. Evid Based Complement Alternat Med. 2014;2014:203173. doi:10.1155/2014/203173. PMID: 25120574.
14. Kami K, Tajima F, Senba E. Activation of mesolimbic reward system via laterodorsal tegmental nucleus and hypothalamus in exercise-induced hypoalgesia. Sci Rep. 2018;8(1):11540. doi:10.1038/s41598-018-29915-4. PMID: 30068977.
15. Lin SC, Lin LL, Lin YT, Chien KL. Evaluating the Effects of Exercise on Inflammation Markers in Musculoskeletal Pain: A Systematic Review and Meta-Analysis. J Clin Med. 2025;14(7):2526. doi:10.3390/jcm14072526. (PROSPERO CRD42024500081).
16. Naugle KM, Fillingim RB, Riley JL 3rd. A meta-analytic review of the hypoalgesic effects of exercise. J Pain. 2012;13(12):1139-1150. doi:10.1016/j.jpain.2012.09.006. PMID: 23141187.
17. Pocovi NC, Lin CC, French SD, et al. Effectiveness and cost-effectiveness of an individualised, progressive walking and education intervention for the prevention of low back pain recurrence in Australia (WalkBack): a randomised controlled trial. Lancet. 2024;404(10448):134-144. doi:10.1016/S0140-6736(24)00755-4. PMID: 38908392.
18. Polaski AM, Phelps AL, Kostek MC, Szucs KA, Kolber BJ. Exercise-induced hypoalgesia: A meta-analysis of exercise dosing for the treatment of chronic pain. PLoS One. 2019;14(1):e0210418. doi:10.1371/journal.pone.0210418. PMID: 30625201.
19. Park SH, Lee MM. The Effects of Resistance Training on Pain, Strength, and Function in Osteoarthritis: Systematic Review and Meta-Analysis. J Pers Med. 2024;14(12):1130. doi:10.3390/jpm14121130. PMID: 39728443.
20. Li Y, Su Y, Chen S, et al. The effects of resistance exercise in patients with knee osteoarthritis: a systematic review and meta-analysis. Clin Rehabil. 2016;30(10):947-959. doi:10.1177/0269215515610039. PMID: 26471972.
21. Andrade A, de Azevedo Klumb Steffens R, Sieczkowska SM, Tartaruga LAP, Vilarino GT. Effects of resistance training on the physical symptoms and functional capacity of patients with fibromyalgia: a systematic review and meta-analysis of randomized clinical trials. Clin Rheumatol. 2023;42(2):553-566. doi:10.1007/s10067-022-06375-w. PMID: 36326999.
22. Maestre-Cascales C, Castillo-Paredes A, Romero-Parra N, et al. Intensity of Resistance Exercise and Its Effects on Pain, Functionality, and Quality of Life in Adults with Fibromyalgia: A Systematic Review. J Funct Morphol Kinesiol. 2025;10(2):121. doi:10.3390/jfmk10020121.
23. Hayden JA, Ellis J, Ogilvie R, Stewart SA, Bagg MK, Stanojevic S, Yamato TP, Saragiotto BT. Some types of exercise are more effective than others in people with chronic low back pain: a network meta-analysis. J Physiother. 2021;67(4):252-262. doi:10.1016/j.jphys.2021.09.004. PMID: 34538747. Ver también: Hayden JA, Ellis J, Ogilvie R, Malmivaara A, van Tulder MW. Exercise therapy for chronic low back pain. Cochrane Database Syst Rev. 2021;9(9):CD009790. doi:10.1002/14651858.CD009790.pub2. PMID: 34580864.
24. Kong LJ, Lauche R, Klose P, et al. Tai Chi for Chronic Pain Conditions: A Systematic Review and Meta-analysis of Randomized Controlled Trials. Sci Rep. 2016;6:25325. doi:10.1038/srep25325. PMID: 27125299.
25. Fernández-Rodríguez R, Álvarez-Bueno C, Cavero-Redondo I, et al. Best Exercise Options for Reducing Pain and Disability in Adults With Chronic Low Back Pain: Pilates, Strength, Core-Based, and Mind-Body. A Network Meta-analysis. J Orthop Sports Phys Ther. 2022;52(8):505-521. doi:10.2519/jospt.2022.10671. PMID: 35722759.
26. Geneen LJ, Moore RA, Clarke C, Martin D, Colvin LA, Smith BH. Physical activity and exercise for chronic pain in adults: an overview of Cochrane Reviews. Cochrane Database Syst Rev. 2017;4(4):CD011279. doi:10.1002/14651858.CD011279.pub3. PMID: 28436583.
27. Pocovi NC, Hancock MJ, Boudreau S, Pinheiro M, Lin CC, French SD. Exercise adherence is associated with improvements in pain intensity and functional limitations in adults with chronic non-specific low back pain: a secondary analysis of a Cochrane review. J Physiother. 2025;71(1):28-37. doi:10.1016/j.jphys.2024.12.001.
28. Davis JM, Bailey SP. Possible mechanisms of central nervous system fatigue during exercise. Med Sci Sports Exerc. 1997;29(1):45-57. doi:10.1097/00005768-199701000-00008. PMID: 9000155.
29. Blomstrand E. A role for branched-chain amino acids in reducing central fatigue. J Nutr. 2006;136(2):544S-547S. doi:10.1093/jn/136.2.544S. PMID: 16424144.
30. Zouhal H, Jacob C, Delamarche P, Gratas-Delamarche A. Catecholamines and the effects of exercise, training and gender. Sports Med. 2008;38(5):401-423. doi:10.2165/00007256-200838050-00004. PMID: 18416594.
31. Leuenberger U, Sinoway L, Gubin S, Gaul L, Davis D, Zelis R. Effects of exercise intensity and duration on norepinephrine spillover and clearance in humans. J Appl Physiol. 1993;75(2):668-674. doi:10.1152/jappl.1993.75.2.668. PMID: 8226467.
32. Chaouloff F. Effects of acute physical exercise on central serotonergic systems. Med Sci Sports Exerc. 1997;29(1):58-62. doi:10.1097/00005768-199701000-00009. PMID: 9000156.
33. Sun LN, Qi JS, Gao R. Physical exercise reserved amyloid-beta induced brain dysfunctions by regulating hippocampal neurogenesis and inflammatory response via MAPK signaling. Brain Res. 2018;1697:1-9. doi:10.1016/j.brainres.2018.04.040. (Estudio representativo del aumento de TPH y receptores 5-HT en rafe dorsal con ejercicio en cinta; ver también Greenwood BN et al., Behav Neurosci 2003).
34. Macfarlane GJ, Kronisch C, Dean LE, et al. EULAR revised recommendations for the management of fibromyalgia. Ann Rheum Dis. 2017;76(2):318-328. doi:10.1136/annrheumdis-2016-209724. PMID: 27377815.

