La pérdida de masa y fuerza muscular se ha convertido en un tema clave en medicina física y rehabilitación, debido a su impacto en la funcionalidad y la calidad de vida.
1. DEFINICIÓN Y EPIDEMIOLOGÍA
La sarcopenia es un síndrome clínico caracterizado por la pérdida progresiva y generalizada de masa muscular esquelética, reducción de la fuerza muscular y deterioro del rendimiento físico, con riesgo significativo de resultados adversos como discapacidad física, mala calidad de vida y muerte. Su denominación proviene del griego: sarx (carne) y penia (pobreza).
El consenso del European Working Group on Sarcopenia in Older People 2 (EWGSOP2, 2018) establece como criterio diagnóstico primario la baja fuerza muscular (siendo el indicador más confiable de sarcopenia), y como criterio confirmatorio la baja cantidad o calidad muscular medida por técnicas de imagen. La baja performance física indica sarcopenia severa.
La prevalencia varía según criterios diagnósticos y población: 1–29% en adultos mayores de la comunidad, 14–33% en residencias de larga estadía, y hasta 10% en pacientes hospitalizados. En Chile, estudios en adultos mayores reportan prevalencia de 15–20% en comunidad.
2. FISIOPATOLOGÍA
La sarcopenia resulta de un desequilibrio entre síntesis y degradación proteica muscular. Los mecanismos subyacentes son multifactoriales e interrelacionados:
2.1 Mecanismos Moleculares
La vía mTORC1 (mechanistic target of rapamycin complex 1) es el principal regulador anabólico. Con la edad y el desuso, se produce resistencia anabólica a la señalización de aminoácidos e insulina sobre esta vía. Paralelamente, se activan vías catabólicas: el sistema ubiquitina-proteasoma (UPS) con sobreexpresión de atroginas MuRF-1 y Atrogin-1, y la autofagia-mitofagia.
La miostatina (GDF-8), factor de crecimiento inhibidor del músculo, aumenta con la edad y el desuso, suprimiendo la proliferación y diferenciación de células satélite. La disminución de IGF-1 muscular reduce la señalización PI3K/Akt/mTOR.
2.2 Inflamación Crónica de Bajo Grado (Inflammaging)
El envejecimiento se asocia a elevación crónica de citocinas proinflamatorias: IL-6, TNF-α, IL-1β. El TNF-α activa NF-κB, promoviendo la transcripción de genes catabólicos y la apoptosis de miocitos. La IL-6 elevada cronicamente tiene efecto catabólico, a diferencia de la IL-6 aguda post-ejercicio que es anabólica (myokine).
2.3 Infiltración Grasa Muscular (Mioesteatosis)
La infiltración de lípidos intramiofibrilares e intermusculares (grasa intermuscular, IMAT) es un hallazgo central en la sarcopenia establecida. Se origina por la transdiferenciación de células satélite hacia el linaje adipogénico (en lugar del miogénico), mediada por la activación del receptor PPARγ. La lipotoxicidad intramuscular genera disfunción mitocondrial, resistencia insulínica local, y amplifica la inflamación mediante DAMPs lipídicos. La mioesteatosis es cuantificable por RMN como fracción de grasa muscular (MFF) y se correlaciona inversamente con fuerza y rendimiento físico.
2.4 Disfunción Mitocondrial
Las mitocondrias musculares envejecidas presentan menor densidad, disfunción de la cadena respiratoria, mayor producción de especies reactivas de oxígeno (ROS) y menor capacidad oxidativa. La biogénesis mitocondrial mediada por PGC-1α está reducida. El estrés oxidativo resultante daña proteínas contráctiles y acelera la proteólisis.
2.5 Denervación Progresiva
La pérdida de unidades motoras tipo II (rápidas) es un mecanismo central. Con el envejecimiento, las motoneuronas alfa de la médula espinal se pierden progresivamente; las fibras huérfanas son reinervadas por motoneuronas tipo I sobrevivientes, resultando en una transición fenotípica de fibras IIx/IIb → tipo I. Esto explica la pérdida desproporcionada de fuerza respecto a masa.
2.6 Alteraciones Hormonales
La deficiencia de testosterona (andropopausia), estrógenos (menopausia), GH/IGF-1 (somatopausia) y DHEA contribuyen a la pérdida muscular. La resistencia a la insulina reduce la captación de aminoácidos y glucosa por el músculo.
3. CUANTIFICACIÓN DE LA PÉRDIDA MUSCULAR POR CONTEXTO
3.1 Pérdida Relacionada con la Edad (Sarcopenia Primaria)
La pérdida de masa muscular relacionada con el envejecimiento sigue un patrón bien documentado en estudios longitudinales:
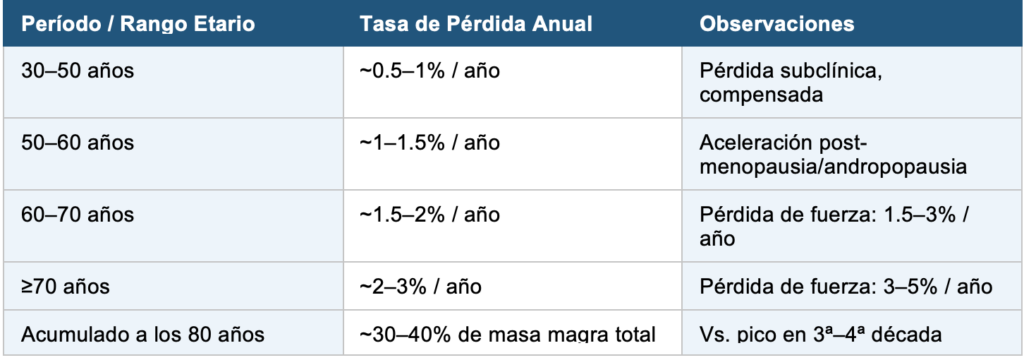
La fuerza muscular se pierde 2–3 veces más rápido que la masa (fenómeno de «disociación fuerza-masa»), reflejando cambios cualitativos: infiltración grasa, desnervación y alteración de la arquitectura contráctil.
3.2 Inmovilismo Extra-Hospitalario
El reposo en cama o la marcada reducción de actividad física en el domicilio produce una pérdida muscular acelerada denominada atrofia por desuso:

En adultos mayores ya sarcopénicos, una semana de reposo en cama puede causar pérdida de masa muscular equivalente a 1 año de envejecimiento normal. La recuperación es incompleta sin intervención activa.
3.3 Inmovilismo Hospitalario
La hospitalización es un potente inductor de sarcopenia aguda. Factores concurrentes: reposo absoluto o relativo, hipercatabolismo por enfermedad aguda, inflamación sistémica, ayuno/restricción calórica, polifarmacia, y resistencia anabólica potenciada por inflamación.

La sarcopenia adquirida en UCI (ICUAW – ICU-Acquired Weakness) es reconocida como una complicación mayor que afecta el 25–60% de pacientes críticos. La miopatía por inmovilismo y la polineuropatía del paciente crítico son sus manifestaciones principales. La ecografía muscular (recto anterior cuádriceps, tibial anterior) es la herramienta más práctica para monitorizar pérdida muscular en UCI.
4. DIAGNÓSTICO Y EVALUACIÓN
El algoritmo EWGSOP2 propone:

La Tomografía Computarizada a nivel L3 es el gold standard para cuantificar músculo esquelético (índice músculo-esquelético L3, SMI) y simultáneamente medir infiltración grasa (densidad muscular en UH). La RMN es superior para cuantificar mioesteatosis. En contexto hospitalario/UCI, la ecografía muscular es la herramienta más práctica (grosor recto anterior cuádriceps, ángulo de penación).
5. MANEJO INTEGRAL DE LA SARCOPENIA
5.1 Ejercicio: Pilar Terapéutico Fundamental
Entrenamiento de Resistencia (ER) — Primera Línea
El ER activa directamente la vía mTORC1 mediante señales mecánicas (mecanotransducción), estimula la síntesis proteica miofibrilar, activa las células satélite, y eleva la secreción de IGF-1 local. Es el único tratamiento que produce hipertrofia muscular real y mejora la calidad del músculo.

En pacientes frágiles o con limitaciones funcionales severas: iniciar con ejercicios asistidos, bandas elásticas, o entrenamiento isométrico. El entrenamiento excéntrico con cargas bajas (Blood Flow Restriction Training – BFR, 20–40% 1RM con manguito oclusivo) es una alternativa validada para pacientes que no toleran cargas altas (postquirúrgico, artrosis severa).
Entrenamiento Aeróbico
El ejercicio aeróbico (caminar, cicloergómetro, natación) activa PGC-1α, mejora la biogénesis mitocondrial, reduce la inflamación crónica y mejora la sensibilidad insulínica muscular. No produce hipertrofia significativa pero mejora la calidad muscular y el rendimiento. Recomendación: 150 min/semana de intensidad moderada (50–70% FCmax), o 75 min de intensidad vigorosa. Idealmente combinado con ER (entrenamiento concurrente).
Ejercicio Multicomponente
Para adultos mayores con sarcopenia, los programas multicomponente (resistencia + aeróbico + equilibrio + flexibilidad) producen los mejores resultados en rendimiento físico, reducción de caídas y calidad de vida. Modelo validado: Programa GLA:D, VIVIFRAIL, OTAGO.
5.2 Nutrición
Proteínas: La Intervención Nutricional Central
La ingesta proteica adecuada es imprescindible para aprovechar el estímulo anabólico del ejercicio. En adultos mayores existe resistencia anabólica que requiere mayor ingesta para lograr síntesis proteica equivalente a adultos jóvenes.

La leucina (aminoácido ramificado) es el principal activador de mTORC1. Dosis umbral: 2.5–3 g leucina/comida. La proteína de suero de leche (whey) tiene el mayor contenido leucínico (~10–11%) y mayor velocidad de absorción. La distribución proteica homogénea en las 3 comidas (vs. concentrada en una sola) optimiza la síntesis proteica diaria.
6. SUPLEMENTACIÓN EN SARCOPENIA
6.1 Creatina — Evidencia de Alta Calidad
La creatina monohidrato es el suplemento con mayor nivel de evidencia en sarcopenia, especialmente en combinación con ER. Sus mecanismos son múltiples y sinérgicos:
- Incrementa los depósitos intramusculares de fosfocreatina (PCr), mejorando la resíntesis de ATP en contracciones de alta intensidad (soporte directo al ER).
- Activa la vía mTORC1 e IGF-1 muscular, estimulando síntesis proteica post-ejercicio.
- Inhibe miostatina y reduce la expresión de genes catabólicos (MuRF-1, Atrogin-1).
- Aumenta la hidratación intracelular del miocito, señal osmótica que promueve síntesis proteica.
- Mejora la función mitocondrial y reduce el estrés oxidativo.
- Efectos neuroprotectores sobre la unión neuromuscular, relevantes en la sarcopenia.

Metaanálisis de Chilibeck et al. (2017, n=1,391): creatina + ER vs. ER solo en mayores de 57 años: mayor ganancia en masa magra (+1.37 kg, 95% CI: 0.97–1.76), fuerza prensil (+1.8 kg), y fuerza tren inferior. Efectos independientes del género.
En contexto hospitalario/UCI: evidencia preliminar sugiere que la suplementación con creatina (5–10 g/día) puede atenuar la pérdida muscular durante el reposo en cama, aunque la evidencia en pacientes críticos aún es en expansión.
6.2 Proteína de Suero (Whey Protein) y Leucina
La proteína whey (25–40 g post-ejercicio o como suplemento entre comidas) es el complemento nutricional más eficaz para la síntesis proteica muscular en adultos mayores. Su alto contenido de leucina (~2.5 g/porción de 25 g) supera el umbral leucínico necesario para activar mTOR. La combinación creatina + whey + ER muestra efectos aditivos en masa y fuerza.
β-hidroxi-β-metilbutirato (HMB): metabolito de la leucina. Dosis: 3 g/día. Inhibe la proteólisis vía UPS y activa mTOR. Metaanálisis muestran beneficios modestos en masa y fuerza, especialmente en sarcopenia severa y reposo en cama. Aprobado por ESPEN para adultos mayores con baja ingesta proteica.
6.3 Vitamina D
La deficiencia de vitamina D (25-OHD < 30 ng/mL, prevalente en >50% de adultos mayores) se asocia a mayor riesgo de sarcopenia, debilidad muscular y caídas. El receptor de vitamina D (VDR) en el músculo regula la transcripción de proteínas contráctiles. Suplementación: 800–2000 UI/día según nivel sérico. Corrección de déficit es mandatoria antes de cualquier intervención en sarcopenia.
6.4 Omega-3
Los ácidos grasos omega-3 (EPA + DHA, 2–3 g/día) tienen efecto anti-inflamatorio muscular y sensibilizan la respuesta anabólica muscular a aminoácidos e insulina (reducen la resistencia anabólica). Metaanálisis 2021 muestran mejoras modestas en masa y fuerza muscular en adultos mayores.
6.5 Colágeno Hidrolizado
15 g/día de péptidos de colágeno, tomados 1 hora antes del ER, ha mostrado en ensayos clínicos (König et al. 2018) aumento de masa libre de grasa, reducción de grasa corporal y mejoría de fuerza en sarcopenia. Mecanismo: estimulación de síntesis de colágeno en tendones/miofascia, mejorando la transmisión de fuerza muscular.

7. ¿PUEDE REVERTIRSE LA INFILTRACIÓN GRASA MUSCULAR EN SARCOPENIA ESTABLECIDA?
Esta es una de las preguntas más relevantes y complejas en el manejo de la sarcopenia avanzada. La respuesta es matizada: la reversión completa es difícil, pero la reducción significativa y funcionalmente relevante es posible con intervenciones combinadas.
7.1 Biología de la Mioesteatosis: ¿Por Qué Es Difícil de Revertir?
La infiltración grasa muscular (IMAT) en sarcopenia establecida tiene dos componentes con distinta reversibilidad:
- Grasa intramiocelular (IMCL): depósitos lipídicos dentro de las fibras musculares como triglicéridos y diacilglicerol. Este componente es metabólicamente activo y relativamente más reversible con ejercicio aeróbico y dieta.
- Grasa intermuscular (IMAT propiamente dicha): tejido adiposo que reemplaza el tejido muscular entre fascículos. Este componente es estructural, corresponde a adipocitos diferenciados, y es significativamente más difícil de revertir. Una vez que las células satélite se transdiferencian hacia el linaje adipogénico (bajo influencia de Wnt inhibido, PPARγ activado), la reversión requiere reprogramación celular.
7.2 Evidencia Sobre Reversibilidad
Los estudios de intervención con ejercicio de resistencia progresivo muestran:
- Mejora de la densidad muscular medida por TC (↑ HU), que refleja menor infiltración grasa intramiocelular, con ER de ≥12 semanas de alta intensidad.
- La ecografía muscular (índice músculo-grasa por escala de grises) muestra mejoría de ecogenicidad con ER sostenido.
- La RMN cuantitativa (fracción de grasa muscular, MFF) muestra reducciones de 10–25% en la fracción grasa con ER + intervención nutricional en estudios de 6 meses en adultos mayores.
- Sin embargo, la IMAT estructural (tejido adiposo intermuscular establecido) no se elimina significativamente con el ejercicio: los adipocitos no se convierten de vuelta en células musculares.
Un punto crítico: el ejercicio anabólico puede no «borrar» los adipocitos infiltrados, pero sí generar nueva masa muscular funcional alrededor de ellos, mejorando la función, la fuerza y el rendimiento, aunque la imagen muscular muestre mezcla de tejido.
7.3 Estrategias con Mayor Impacto sobre Mioesteatosis
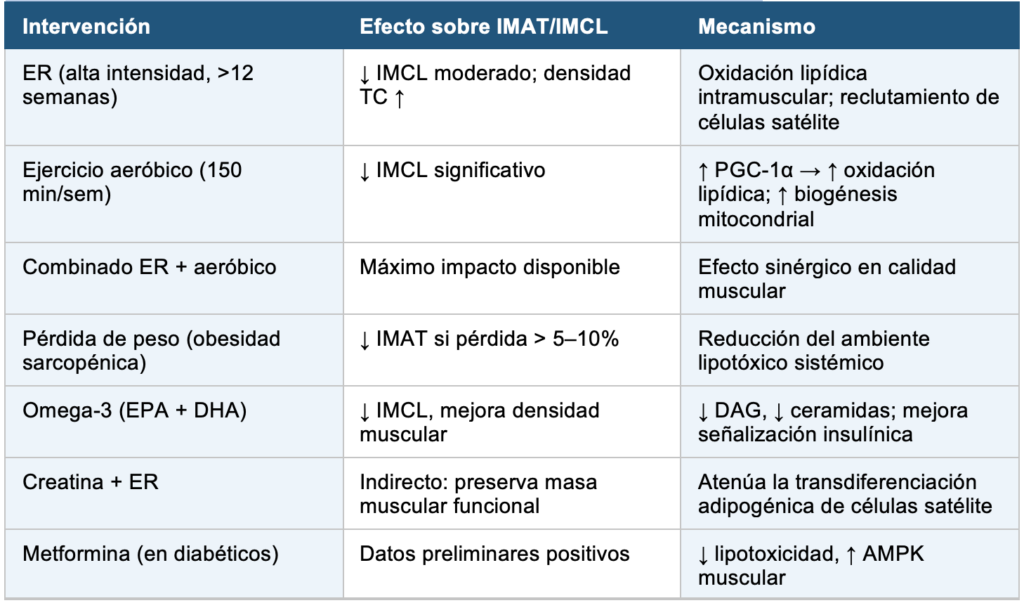
7.4 Respuesta Directa a la Pregunta
La infiltración grasa muscular en sarcopenia establecida: ¿se puede revertir?
Respuesta basada en evidencia actual (2024):
- La grasa intramiocelular (IMCL) es parcialmente reversible con ejercicio aeróbico + resistencia sostenido + corrección nutricional. Estudios de 6–12 meses muestran reducciones de 15–30% en IMCL cuantificado por espectroscopía RMN.
- La grasa intermuscular (IMAT estructural, adipocitos diferenciados) tiene reversión muy limitada con los tratamientos actuales no farmacológicos. No existe intervención clínica validada que elimine significativamente el IMAT establecido.
- Sin embargo, la relevancia clínica es que la función muscular puede mejorar significativamente incluso sin reducción estructural del IMAT, mediante la generación de nuevo tejido muscular funcional (hipertrofia adaptativa de las fibras residuales) y mejora de la calidad contráctil.
- La prevención es más eficaz que la reversión: intervenir en estadios tempranos (pre-sarcopenia, sarcopenia inicial) antes de que el IMAT esté establecido produce mejores resultados morfológicos y funcionales.
Perspectivas futuras: inhibidores farmacológicos de adipogénesis muscular (inhibidores de PPARγ, activadores de Wnt muscular como anti-miostatina, ACVR2B-inhibidores) están en investigación clínica fases II–III como potenciadores del efecto del ejercicio.
8. ALGORITMO CLÍNICO PRÁCTICO
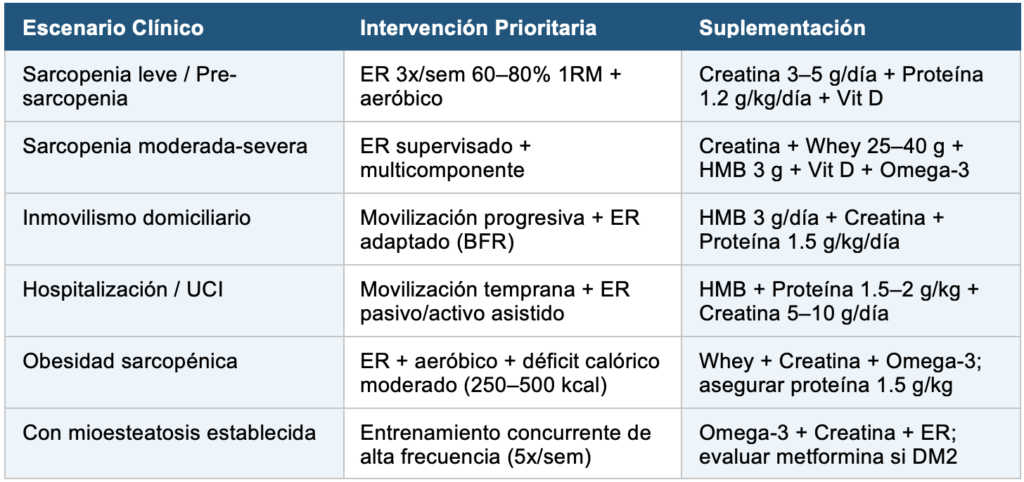
9. CONCLUSIONES
La sarcopenia es una enfermedad muscular con consecuencias sistémicas que resulta de mecanismos biológicos complejos acelerados por el envejecimiento, el desuso y la enfermedad aguda. La pérdida muscular varía desde 0.5–1% anual en adultos de mediana edad hasta 2–3% en mayores de 70 años de forma fisiológica, con tasas dramáticamente superiores en inmovilismo (0.5–1% por día de reposo) y en UCI (hasta 2.5% del cuádriceps por día).
El ejercicio de resistencia progresivo es el único tratamiento con evidencia de nivel A para revertir la sarcopenia, con la creatina monohidrato como el suplemento con mayor respaldo científico en combinación con ER. La proteína adecuada (1.2–1.6 g/kg/día), vitamina D y omega-3 completan la intervención nutricional.
La mioesteatosis establecida tiene reversibilidad limitada, especialmente su componente estructural (IMAT). Sin embargo, la función muscular puede mejorar significativamente mediante generación de nueva masa funcional y mejora de calidad contráctil. La intervención temprana, antes de que la infiltración grasa esté consolidada, ofrece los mejores resultados morfológicos y funcionales.
La integración de la evaluación de sarcopenia como práctica rutinaria en la valoración funcional del paciente hospitalizado, y el inicio precoz de movilización y soporte nutricional, son estrategias con alto impacto en resultados clínicos y calidad de vida.
REFERENCIAS CLAVE
Cruz-Jentoft AJ et al. Sarcopenia: revised European consensus on definition and diagnosis. Age Ageing. 2019;48(1):16–31. (EWGSOP2)
Puthucheary ZA et al. Acute skeletal muscle wasting in critical illness. JAMA. 2013;310(15):1591–600.
Chilibeck PD et al. Effect of creatine supplementation during resistance training on lean tissue mass and muscular strength in older adults: a meta-analysis. Open Access J Sports Med. 2017;8:213–26.
Dent E et al. International Clinical Practice Guidelines for Sarcopenia (ICFSR). J Nutr Health Aging. 2018;22(10):1148–61.
Bhasin S et al. Sarcopenia Definition & Outcomes Consortium Report. J Am Geriatr Soc. 2020.
Goodpaster BH et al. The loss of skeletal muscle strength, mass, and quality in older adults: the health, aging and body composition study. J Gerontol. 2006;61:1059–64.
Addison O et al. Intramuscular fat and associations with metabolic risk factors in the Health ABC Study. Obesity. 2014;22(7):1696–703.

